前言
「老化」是個神秘的過程,而且引發了我們許多疑問。為何生物會老化?為何我們死亡的年齡又各有不同?老化背後又蘊藏著什麼機制?科學家觀察到,一組實驗室小鼠即使基因相同,每隻壽命卻各有不同,令人嘖嘖稱奇。當生物老化時,細胞功能失常的情況會增加,影響正常組織功能,導致與年齡相關的疾病形成,如癌症、神經退化性疾病、心血管疾病 (CVD)。全球人類平均預期壽命大幅提高,部分原因來自治療、診斷和醫療體系的進步。隨著人類壽命延長,對老年人的照顧亦加重了醫療體系的負擔,皆因老化會伴隨著很多與年齡相關的缺陷或問題;另外,勞動人口老化亦導致生產力降低的問題。老年人的共同特徵是越接近八十歲,衰弱會越變得明顯,以及容易罹患腦退化症。為何老化會離不開這些缺陷?人類有沒有辦法跨越這些缺陷,甚至邁向長生不老?
我們目前對老化的大部分理解都來自對動物及單細胞模型所作過的研究,例如實驗室小鼠、線蟲(即秀麗隱桿線蟲,學名Caenorhabditis elegans,簡稱C.elegans)及酵母(即釀酒酵母,學名Saccharomyces cerevisiae,簡稱S.cerevisiae)。儘管已有大量對老化的研究,但我們對此的理解仍然有限,因為這些動物模型只模擬了老化某些方面的特徵,所以我們對上述問題仍然是無從入手。希望本文能引領讀者了解「時間上」的老化與「生物上」的老化概念有何不同︰前者是指由出生至某個日期所經過的時間長度;後者是指生物體的細胞逐漸累積不可逆轉的損傷(例如 DNA、蛋白質、脂質等大分子)。本文會從某些老化的特徵探討生物老化,以及我們可以透過什麼途徑減慢衰老,從而活出長壽而豐富的人生。
老化的跡象
遺傳不穩定性
老化與生物在一生裏積累的遺傳物質損傷有密切關係。在細胞分裂過程中,細胞機器會複製細胞基因組,然而這個過程容易出錯,因而導致基因突變發生以及更多活性氧類 (ROS)的產生,與化學物質(例如紫外線輻射)接觸亦可能引致 DNA 損傷。根據 DNA 損傷的類型,細胞可透過啟動細胞週期檢查點(checkpoint)來作出反應,從而暫停細胞週期,讓細胞有時間進行 DNA 修復,並在有需要時啟動分解蛋白質的一連串化學反應。細胞具有多條DNA 修復路徑,這對保持細胞基因組完整至關重要,並且被認爲在維持壽命方面發揮了重要作用。事實上,DNA 修復過程中的幾種遺傳缺陷正是與幾種早衰症有關。
老化與生物在一生裏積累的遺傳物質損傷有密切關係。在細胞分裂過程中,細胞機器會複製細胞基因組,然而這個過程容易出錯,因而導致基因突變發生以及更多活性氧類 (ROS)的產生,與化學物質(例如紫外線輻射)接觸亦可能引致 DNA 損傷。根據 DNA 損傷的類型,細胞可透過啟動細胞週期檢查點(checkpoint)來作出反應,從而暫停細胞週期,讓細胞有時間進行 DNA 修復,並在有需要時啟動分解蛋白質的一連串化學反應。細胞具有多條DNA 修復路徑,這對保持細胞基因組完整至關重要,並且被認爲在維持壽命方面發揮了重要作用。事實上,DNA 修復過程中的幾種遺傳缺陷正是與幾種早衰症有關。
粒線體功能的變化
粒線體是以ATP形式產生能量供細胞執行日常功能的主要細胞器官。它們具有遺傳自母親的 DNA,進行ATP合成作用時亦會產生活性氧類 (ROS) 作為副產物。粒線體 DNA (mtDNA) 容易出現與衰老相關的突變,部分原因是活性氧類的釋放以及缺乏組蛋白保護 DNA 免受損傷。此外,粒線體中DNA 修復路徑的效能亦會低於細胞核中的路徑。這些突變更常在年老細胞中出現,並會影響呼吸鏈複合物的功能(其功能是在不同組織中產生 ATP)。當小鼠因為突變而缺少一種粒線體酶時(其功能是複製粒線體 DNA,mtDNA),會出現過早衰老及壽命縮短。科學家在老化人類的心臟、大腦和肌肉中也發現 mtDNA 缺失,進一步證明了維持 mtDNA 的穩定是決定老化能否健康正常的關鍵。
呼吸鏈蛋白的功效會隨著老化而下降,導致電子的洩漏增加以及 ATP 的產量減少。功能失常的粒線體可能會受到其薄膜穩定性及粒線體動態變化的影響。細胞可以透過粒線體自噬(即粒線體被囊泡「吞噬」並分解)來去除有缺陷的粒線體。粒線體自噬功能的缺陷往往與阿茲海默症 (AD) 及其他神經退化性疾病有關。研究亦發現,端粒的維護有助促進粒線體自噬。當小鼠缺乏端粒酶,粒線體的數量及生長亦降低,從而影響細胞中粒線體的正常功能。當研究人員激活端粒之後,粒線體衰退得到部分逆轉。科學家們指出,老化過程中逐漸出現的粒線體功能失常或會增加 ROS 水平(ROS 會降低細胞器正常運作的能力)。然而他們又發現,ROS 的增加亦延長了壽命,而提高抗氧化物亦無助於延長動物的壽命,與上述理論有衝突。但無論如何,粒線體功能失常已肯定是老化跡象之一。
端粒長度
如前面所述,DNA 損傷的增加與年齡有關,其端粒(位於染色體末端)會變得非常脆弱。DNA 損傷可能導致細胞凋亡或衰老。複製酶亦無法完全複製端粒,這只能依賴端粒酶的活性。然而,多數哺乳類動物的細胞並沒有端粒酶,以致端粒逐漸縮短。而且,這些位置的 DNA 修復亦受到很大的限制,因為它們一般都結合了蛋白質,以免端粒在正常情況下被當作受損的 DNA。研究發現,端粒的缺陷與人類疾病的早期發展有關。缺乏端粒酶的動物模型壽命較短;當啟動端粒酶後,壽命則會延長。另外需要留意的是,最近一項對癌症相關突變的研究發現,長端粒似乎會增加人類患癌的風險。端粒縮短雖然與早衰老有關,但亦有助預防癌症,因為它可以阻止細胞分裂。總而言之,端粒長度並非量度細胞年齡的可靠標準。
衰老
衰老是指不可逆轉地離開細胞週期的狀態,或會隨細胞應激(cellular stress)而發生。要辨認衰老細胞,可借助一組由衰老細胞分泌的蛋白質,稱為「衰老相關分泌表型」(senescence-associated secretory phenotype,SASP)。 這類分泌出來的因子,如生長因子、炎性細胞因子和酶,可影響鄰近細胞的生長。這些細胞可以被識別,是因為它們所呈現已知蛋白質的量與CVD 及 AD等衰老相關疾病所表現的相當。若在顯示衰老跡象的早衰動物模型中去除這些蛋白質,可以改善受影響細胞的狀態。由於在老化過程中衰老會加劇,因此衰老被認為會導致老化。然而,從小鼠身上又見到,當衰老相關蛋白質小幅度增加時,壽命會延長。這項觀察顯示,這些蛋白質的初期累積可能是細胞的反應方式之一,但過度的衰老又反而會減弱細胞功能。
蛋白質穩定狀態的問題
我們已肯定老化與蛋白質穩定狀態受損有關。穩定狀態是指細胞透過一系列品質控制(QC)路徑來維持細胞環境穩定的能力,藉此確保蛋白質摺疊正確以及功能失常的蛋白質能充分地被移除。在蠕蟲和蒼蠅中,這些 QC 相關蛋白的高水平導致了壽命延長。蛋白質要正常發揮作用,就必須摺疊正確,而在苛刻的條件下,蛋白質會發生聚集。研究發現,錯誤摺疊的蛋白質與老化相關疾病有關,例如 AD 及帕金遜症。
自噬-溶酶體路徑對維持蛋白質穩定狀態亦很重要。這個「自我吞食」的過程能透過將目標與含有消化酶的囊泡融合來將內容物降解,從而將細胞中功能失常或不必要的細胞成分去除。然而,自噬會隨著年齡減慢,這被認為與神經退化性疾病及癌症有關聯。使用藥物可以增加自噬,從而延長酵母及線蟲的壽命,並延緩小鼠的某些老化跡象。總括而言,蛋白質喪失穩定狀態是衰老相關疾病的共有特徵,因此可能成為未來抗衰老治療的目標。
成體幹細胞功能
成體幹細胞 (ASC) 對維持組織功能及整體健康有重要作用。它們位於特定的組織之中,例如腸道、骨髓、肝臟和骨骼肌肉。成體幹細胞一般負責組織的維護及恢復,其中一部份會處於靜止狀態(未進入細胞週期),因此可以快速回應刺激(例如組織損傷)、啟動並重新進入細胞週期。一個幹細胞會分裂成兩個子細胞。其中一個子細胞會被指定分化成構成該組織的多種細胞之一;另一個子細胞則會以幹細胞形式返回靜止狀態。這個機制可保護 ASC 免於 DNA 損傷並維持常駐幹細胞的數量。然而,隨著年齡增長,ASC 會開始失去啟動能力,因而降低組織的再生能力。此時 ASC 會出現異常的細胞分裂並無法恢復靜止狀態,因此會消耗幹細胞庫,以致某些情況下,老年生物體的幹細胞比年輕生物體少。
骨髓、肝臟、脾臟的其中一組幹細胞是為造血幹細胞 (HSC)。HSC 是學術界已充分研究的 ASC 之一。HSC 會在造血作用(hematopoiesis)中產生血細胞(包括紅血球及免疫細胞)。這個過程會隨著年齡增長而減慢,導致免疫細胞及血細胞減少,最終導致免疫系統變弱、抵抗感染的能力降低,增加貧血發生率以及患癌的風險。年老囓齒動物模型中的 HSC 顯示,其細胞週期活性降低及再生能力降低。
突變可以在幹細胞中進行整理。白血病相關突變的研究發現,在正常血細胞身上,與白血病無關的突變普遍比預期更多。血細胞在很大程度上被認爲是源自年青成人體內的一千個活躍幹細胞,然而當這些血細胞之中又有許多都帶有相同的突變時,可以推斷在某些人的身體裡這些血細胞是由單一幹細胞負責演變而成的。這個現象在老年人中越來越常見,它與心血管疾病、中風、糖尿病風險增加有關。科學家在這些幹細胞中發現了一些突變基因,而這些基因通常負責編碼製造控制基因表達的蛋白質。模擬不同血病的小鼠模型大部份都有幹細胞突變,導致幹細胞無法維持。一條在正常條件下調節對壓力及 DNA 損傷反應的基因普遍地在癌症中發生突變,但又控制著 HSC 細胞分裂。當缺少該基因的 HSC 被移植到其他生物體時,它們會減少細胞分裂,再生組織的能力會下降。
骨骼肌由位於肌肉纖維基底層(basal lamina)之下的肌肉幹細胞(又稱為衛星細胞 (SCs))組成。當受傷後,SCs 對受傷後的肌肉再生發揮主要作用。然而,由於幹細胞分裂能力降低,年老肌肉的再生過程會減慢,因此幹細胞分化成新肌肉纖維的速度會減慢。 SCs 亦對周圍環境相當敏感,它們正常運作的能力容易受到影響。眾所周知,老化的變化會改變微環境,從而導致肌肉流失。人類在老化過程中的肌肉質量及強度喪失的情形又稱為少肌症,會增加跌倒、身體殘疾和死亡的風險。少肌症的生物原理尚未清楚,但一般認為與多種因素有關,例如炎症、粒線體功能異常、肌肉結構喪失、幹細胞數量減少。

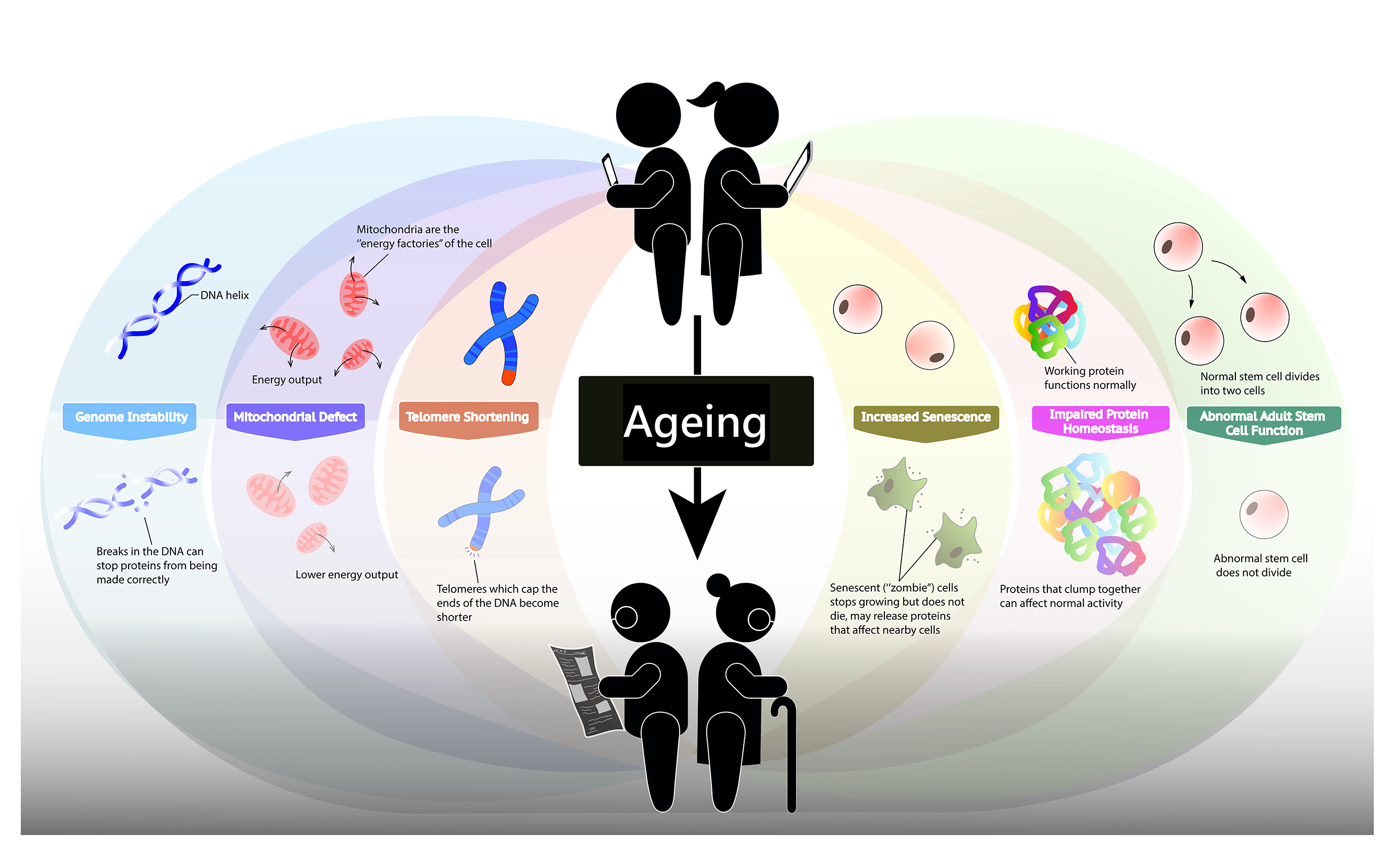
圖一:老化的跡象
老化過程的未解之謎
我們普遍認為,衰老過程是所有生物的結果,當年齡增長,死亡率就會增加。生物體能否在成年期確保功能健全,取決於體內穩定狀態,因此必須予以嚴格調節;否則可能會導致細胞功能失常,繼而出現疾病。然而,有幾項重要的實驗改變了我們對老化的認識。聯體共生是指利用手術將兩個生物體(一個年輕,一個年老)聯合為一的過程,以便我們研究血液中與年齡相關及疾病相關變化。暴露於年輕環境的年老幹細胞表現出較年輕的特徵,可見要恢復某些年老特徵是有可能;暴露於年老環境的年輕幹細胞則表現出與老化相關的細胞功能缺陷,顯示幹細胞會深受環境影響,而釋放到血液中的因子可能是逆轉老化的關鍵。
研究人員在聯體共生實驗中發現幾種老化相關血液因子是與炎症或免疫系統相關的蛋白質,例如是影響神經元細胞生長及分裂的細胞因子。其他蛋白質的水平亦會隨年齡增加,甚至影響肌肉組織的再生。總而言之,實驗反映炎症在老化過程中有某些作用。
返老還童的實驗來自研究精子令卵子受精的過程;受精過程中,兩個細胞會二合為一,形成一個不帶有任何親代細胞年齡痕跡的單一細胞。有較早的實驗從蝌蚪的肌肉取出細胞核並轉移至移除了細胞核的滑爪蟾(Xenopus)卵中,生出健康的雄性及雌性青蛙,顯示細胞核被卵子的環境以某種方式重編程。從一些對年輕及年老細胞分子特徵的研究可見,雖然所有細胞都攜帶相同的基因組 DNA,但基因轉錄受表觀遺傳學所控制,因此基因相同的細胞會成為不同類型的細胞。

圖二:表觀遺傳學
表觀遺傳學是指在DNA序列不改變前提下,透過染色質、DNA、RNA、蛋白質結構的化學變化而發生的基因表達變化。DNA 是由單一核苷酸單元組成的一條長鏈,可利用化學方法予以修飾。科學家已清晰呈現兩種化學變化:利用特定的酶將胞嘧啶甲基化(在某些核苷酸上出現)及將賴氨酸乙酰化(在組蛋白上出現),達到改變基因表達的目的。在特定基因組位置增加組蛋白的乙酰化或三甲基化,可造成我們所謂的年齡相關表觀遺傳學標記,而在聯體共生過程中去除這些標記,可使年老細胞恢復至年輕、健康的細胞。
科學家極想了解哪些細胞路徑導致基因表達控制失調,從而導致老化過程中幹細胞功能下降。在無脊椎動物模型中顯示,組蛋白甲基化與衰老有關,而當引致甲基化增加的基因發生缺失時,會令延長壽命的表型出現。研究亦發現,與推動基因表達的啟動子(promoter)相關的一個特定組蛋白甲基化標記出現時,與壽命縮短有關聯。相反,在酵母中,當其另一種組蛋白標記的水平下降時,壽命則減少。研究人員利用DNA甲基化來作老化生物標記,估計整個人類生命週期間的組織年齡。此外,在一些比較人瑞(達百歲者)與中年人的研究中,科學家發現甲基化基因會發生變化,而部分基因與疾病有關聯。
有什麼方法可以防止衰老?
目前市場上並無抗老化的藥物可供使用,然而研究已充分證實環境因素對改善細胞健康的益處。動物模型的研究證實,卡路里限制 (CR) 可增加壽命,其部分原因是促進自噬以及脂肪的代謝,從而降低體重。可是人類始終難以維持 CR,因此營養學家提出間遏斷食法 (IF),即在一日的連續八小時之內進食,在剩餘十六小時之內則斷食。IF 亦能改善自噬、提高葡萄糖耐受性,並幫助身體由葡萄糖轉換至以酮為能源進行代謝。
有趣的是,CR亦減少了恒河猴體內的年齡相關DNA甲基化變化。因此,對處於糖尿病前期以及肥胖的人士,CR 及 IF 是有效的手段。採用某些飲食法亦有其好處,正如早有研究發現地中海飲食與長壽和預防心血管疾病及癌症有關。這種飲食法的特點是進食大量蔬菜、植物性食物、水果、魚、橄欖油,同時提高維他命、抗氧化物、omega-3 脂肪酸的攝取量,這些營養素均有助改善細胞健康。
運動或體力活動對人體的健康亦非常有益,例如可改善心血管健康及增強骨骼肌肉。在有關肥胖的臨床研究及實驗模型亦顯示,運動有理想的效果。在進行帶氧運動的小鼠中,其組織中的自噬增加,包括骨骼肌肉、心臟、肝臟。長期運動亦使小鼠的高脂肪誘導葡萄糖耐受不良改善。運動對幹細胞功能的益處亦在小鼠身上得到證明。在研究中,研究員向小鼠提供一個跑步滾輪,年老小鼠在跑步後肌肉修復加快,而其 SC 功能相比年輕幹細胞亦有改善。運動亦部分逆轉了老化過程中的轉錄變化,並緩和了年老肌肉幹細胞中的一些細胞應激跡象。研究亦發現,抗阻力運動可增強肌肉質量及強度,在年輕少肌症病人身上有相同益處,顯示其實可透過外部方法恢復失去的肌肉質量。
運動的其他好處包括增加粒線體的生物合成、增強骨骼肌肉中的 ATP 產量,以及促進粒線體自噬。有氧運動除了對心血管有益處外,運動亦能透過增加生長因子的分泌來促進神經元健康,從而支持已有的和新的神經元生存,並支持學習及記憶的過程。有一項對輕度認知障礙病人的試驗顯示,他們進行有氧運動後,海馬體收縮減少、大腦功能改善,記憶力提升。
總結
現時全球的老年人口比例越來越高,特別是在醫療保健及社會服務較佳的發達國家。人類死亡的主要原因是老年患病,因為通常老人對疾病感染的抵抗能力較低,而且身心健康狀況較差。然而,有些老人仍然生活得很有活力,而且長命百歲。難道延緩衰老的秘密就藏在這少數人身上?我們所知的是環境因素,例如生活方式,可以影響細胞正常運作的能力,以及可能在一定的基因層面上減緩老化的表現。然而,我們對於老化的生物學理解仍然有很多不明之處,這點會更加激發科學家研究老化,務求最終能研發出令人類即使變老亦能改善健康質素並得享長壽的方法。
術語解釋
癌症:一組涉及不受控制的細胞生長,並會形成腫瘤的疾病。
神經退化性疾病:一組涉及神經細胞死亡或功能異常的疾病。
心血管疾病 (CVD):涉及心臟或血管功能異常的疾病。
衰弱:體質虛弱,老化的常見徵狀。
腦退化症:泛指喪失記憶或其他腦功能,使日常生活受影響。
基因突變:DNA序列發生變化。
活性氧類 (ROS):不穩定的含氧分子,可與 DNA、RNA 或蛋白質起反應,造成損害。
細胞凋亡:一個導致細胞死亡的有序過程,描述了組織如何去除癌細胞或功能失常的細胞。
衰老:細胞開始功能衰退並停止分裂的不可逆轉狀態。
ATP:三磷酸腺苷,一種供細胞用作執行日常功能的能量攜帶分子。
組蛋白:包在 DNA 裏的蛋白質,一般會保護 DNA 免受損傷。
阿茲海默症 (AD)︰俗稱老人痴呆症,一種無法治癒的腦部疾病,成因是神經元死亡或功能異常,影響記憶及思維能力。
粒線體自噬:通過降解方式去除細胞內受損粒線體的過程。
囊泡:攜帶細胞物質的細胞之內/外部結構。
抗氧化物:抗衡 ROS 的化學物質,又稱為「自由基清道夫」,通常具保護作用。
端粒酶:維持端粒穩定的酶。
端粒:位於 DNA 的末端,保護 DNA 不與其他 DNA 融合。
帕金遜症 (PD):腦疾病,成因是神經元死亡或功能失常,導致顫抖、僵硬及行動困難。
自噬:細胞去除不需要或機能失調成分的自然過程,又稱為「自食」。
分化:細胞由某種類型變成另一種類型。
靜止:細胞處於如非必要不會分裂的可逆轉狀態,見於成體幹細胞(非休眠狀態)。
白血病:一種白細胞癌症。
中風:流向大腦的血因為出血或血管受阻而被隔斷,導致細胞死亡。
糖尿病:血糖維持高水平的疾病,導致血液裏的血糖積聚。
少肌症:骨骼肌肉質量及強度會緩慢喪失的疾病,多見於老人。
聯體共生:實驗方法,將兩個生物體連至一套共同生理系統(例如筋膜、供血系統)。
炎症:身體組織對有害刺激(如感染、組織損傷)的生物反應。
細胞因子:炎症時細胞釋出的一大組蛋白質,作用是向其他細胞發出信號。
表觀遺傳學:對DNA序列不改變前提下,基因表達變化的研究。
甲基化:將-CH3 基團添加至化合物中的化學過程。當添加至 DNA 或組蛋白時,會控制基因表達。
乙酰化:將-OOH基團添加至化合物中的化學過程。當添加至組蛋白時,會控制基因表達。
賴氨酸:鹼性氨基酸,是蛋白質的組成部分。
核苷酸:DNA 和 RNA 的組成部分。
胞嘧啶:構成 RNA 和 DNA 的四種化學鹼基之一。
生物標記:反映可能有疾病跡象的可測量的變量。
卡路里限制 (CR):減少食物攝取量至低於每日卡路里攝取量。
酮:脂肪酸分解後釋放的分子,可在禁食或劇烈運動後釋出。
輕度認知障礙 (MCI):泛指思維能力持續喪失的大腦狀況,會增加晚年患上 AD 的風險。
作者簡介
張曉東教授現為香港科技大學(HKUST)生命科學部的何善衡生命科學副教授。張教授在美國科羅拉多大學獲得生物化學博士學位。他的研究專長是幹細胞及老化生物學,曾利用實驗室老鼠的肌肉幹細胞發現幹細胞靜止及組織再生的關鍵分子路徑。張教授亦因「幹細胞衰老過程中的分子控制」研究獲得 2015 年裘槎前瞻科研大獎,並曾在著名期刊發表超過三十篇科學論文。此外,張教授亦擔任香港科技大學 – 南豐集團聯合實驗室主任、生物科學實驗中心副主任、香港科技大學 – 華大基因聯合研究中心主任、香港科技大學 – 上海第六人民醫院腦科學聯合研究中心副主任,以及位於香港科學園的香港神經退行性疾病中心 (HKCeND) 的主要成員。
Erin Tse博士在英國阿斯頓大學獲得生物醫學科學博士學位,在 Eric Hill 博士的指導下研究阿茲海默症。謝博士為求有更高發展而移居香港,從事微生物學研究,隨後加入病毒學小組一段時間,利用由人類幹細胞衍生的類腸道組織研究人類諾沃克病毒結構蛋白的宿主互作。謝博士憑藉其學術經驗,專門從事細胞生物學的研究。謝博士目前是張教授實驗室的博士後研究員,並將在此繼續其幹細胞研究。謝博士亦是香港科技大學 – 南豐集團聯合實驗室的活躍成員,主要負責管理聯合實驗室的活動及指導學員。
2022年3月