我们都来自哪里?「Stammbaum」与「Stammzelle」
创造今天世界上形形色色、精彩绝伦的动物生命形式时,所需要的是什么?人类之所以成为人类的关键步骤是什么?我们的根源在哪里?这些问题迷倒了科学家、医生、哲学家、学者等众多人士。英国著名博物学家达尔文 (Charles Darwin) 改变了我们对自然历史的思考方法。他提出了一种具条理的生命进化理论:在每一个物种的每一代族群里,都会存在某些变异,当中一些变异或许是正面的,另外一些则可能是负面的。由于有这些变异,族群中的某些成员会比另外一些成员更加容易生存,并且能够更有效地繁殖后代。久而久之,这种最能够切合特定环境的个体的自然选择过程便会导致演化出新的生命形式和物种。德国生物学家、艺术家兼哲学家海克尔 (Ernst Haeckel) (1834-1919) 对达尔文的思想深为折服之余,更进一步发展和普及了进化论这个概念,可是,这个概念却遭到了当时社会各界的坚决反对。同一时期,德国的威玛公爵思想开放,而且是多种艺术和科学事业的赞助人,更吸引了席勒 (Friedrich Schiller) 和歌德 (Johann Wolfgang Goethe) 等人物。海克尔就是在威玛公爵的支持下,在耶拿大学城工作(图 1)。海克尔采用在德文里称为「Stammbaum」的家谱树或系统进化树的方式来阐述生命的历史(Stamm:即是茎或动物门的意思)。根据这个概念,所有生命形式都有一个单一的主干,然后分支出去,并各自进化成为过去和现在居于地球上多如繁星的各种动物。那么,「Stammbaum」的根源是什么?什么是所有动物的共同祖先?与这个概念相关的是,海克尔提出了「生物发生律」。这个学说提出,每种生物体的发育正是反映了其进化历史的一个快速而浓缩的版本(「胚胎的发育过程重演了原始生物进化的步骤」)。这个概念引发了所有细胞都有一个祖细胞的想法。[1, 2] 所有动物都是从单一个细胞 — 受精卵 — 发育而来。它的「种质」从一代流传至下一代(「种质」这个概念最先源于韦斯曼 (August Weissmann),其后人们才知道 DNA 才是遗传讯息的载体)[3]。因此,每一种动物都可以追溯到一个单细胞受精卵,并且根据系统发育家族史,所有动物都是源於单一细胞。这个细胞是「Stammbaum」的最终种子,也是我们的共同祖先。海克尔在他的 1868 年著作《自然创造史》(Natürliche Schöpfungsgeschichte) 里,自创了这个我们现在用来形容具有非常特殊性质的细胞的术语。他又使用了德文里的「干」一词,将处于我们的个体发生的基础位置之细胞,以及所有动物生命的共同祖先之系统发生类比称为「Stammzelle」,也就是「干细胞」。[3]

图1:— 海克尔在 19 世纪创造了「干细胞」一词。照片中的是至今仍保存在德国耶拿的海克尔书房( Ralf Jauch 摄)。
干细胞是什么?
这个词语在现代的含义已经偏离了动物界所有细胞的高曾先祖这个原始意义。干细胞有两个重大特性。首先,干细胞可以自我复制,并且无限繁衍。换句话说,一个干细胞可以产生更多的干细胞,基本上它是永生的。第二,当干细胞接到指令时,可以转变为在体内发挥特定作用的特殊细胞类型。我们可以凭干细胞的效能来区分它们。受精卵是全能的,这表示它有能力发育成为完整的生物体,并且可以形成一个可存活的胚胎。随著细胞分裂,它们逐渐形成具有专门功能的细胞。当发育中的胚胎植入子宫时,它包含一个球形的好像囊肿的结构,当中具有三种主要类型的细胞。其内部则包含大量的多能干细胞,这些干细胞可以形成所有的身体细胞,但不能形成胚胎周围的细胞,例如胎盘。成年动物仍然有干细胞,但这些干细胞的效力仅限于特殊的身体组织和器官。举例说,神经干细胞只能形成神经系统的细胞。
干细胞在动物演进里发挥的作用
植物、真菌、动物都是由真核细胞组成的,并独立发育出多细胞性。从单细胞真核生物(原生生物)到复杂的多细胞动物的转变,在我们本身的进化史上,属于一项破天荒的举措。我们对具有有限数目的细胞类型的动物(例如海绵)进行的研究,以及与今天仍然存在于我们周围的动物的单细胞亲戚(例如领鞭毛虫)进行之比较,都影响著我们对于上述转变是如何发生之想法。单细胞生物的细胞可以暂时地改变身份,有时更会形成类似于多细胞实体的细胞聚集体。各种动物都是由特殊的细胞类型组成,这些细胞类型共同构成一个经精心安排地协同工作的单位。例如人类就有大约 200 个高度特化的细胞和一整套复杂的器官系统。它们的核心就是控制新细胞的形成之干细胞。一些动物例如扁盘动物或海绵,其细胞种类有限,缺乏神经系统或肌肉。至于所有动物的单细胞的祖细胞是什么样子的,以及它需要经过哪些演化才能过渡成为我们的多细胞祖先?要检索出这些脆弱的实体的化石记录已近乎不可能。但是,藉著研究当今大自然在生命之树的不同分支上使用了哪些分子工具包,便可以更好地理解和推断出我们所起源的细胞使用了哪些分子。
生命的分子及其保护
让我们的细胞得以发挥作用的分子机制显示出惊人的保护水平,这有力地证明了生命具有共同的根源。遗传密码是普遍适用的,遗传讯息在生命的不同领域里的翻译和复制方式都非常相似。找出是什么样的演化性创新使新的生命形式得以形成,就是理解我们的自然史的关键。虽然我们无法回到过去,手上也没有化石记录或者保存下来的数亿以至数十亿年前存在的生命形式的遗传物质痕迹,但是,我们可以比较现存物种的基因,并且重建我们共同祖先可能使用过的分子工具。如果某些特定基因乃某个特定生命分支所独有,那么,那些特定基因便可能是引领至该个分支的演化路径上的一个独特发明,并且可能是其祖先物种进行演化所必需的。
原生生物变成动物的必需因素
科学家们认为,出现第一个复杂真核细胞这项重大改变事件乃在大约 20 亿年之前发生。在此之后,又经历了 10 至 15 亿年的进化修补,才有第一批动物出现。看来,为了形成以植物、微生物或其他动物为食物的更为复杂的多细胞生命形式,当中所需的分子创新绝非微不足道。我们现在已知道许多动物及其单细胞近亲的基因组。丝状鞭毛虫和领鞭毛虫是与动物有最相近关系的单细胞水生原生生物。藉著研究它们的生命周期和它们的基因,有助我们了解创造动物时需要哪些飞跃。将多个细胞凑合在一起所需的基因,也就是帮助细胞进行沟通和接收讯号的因素,可能就是动物专用而动物的单细胞亲戚所缺乏的主要分子工具。在动物的发育过程中打开和关闭基因,从而为细胞身份进行定义、为细胞命运对话进行编程的分子开关,也可能是动物独有的进化创新。但是,我们越是深入地调查我们的单细胞亲戚的基因库,发现真正的动物特有基因和路径种类就越少。从基因角度看,在动物进化之初,并没有出现新生基因的爆发。相反,只出现了一个较小的新基因组合,而触发第一种动物的出现之进化飞跃的生命蓝图整体变化则相对细微。
为多能干细胞作定义的基因
在 1980 年代和 1990 年代,科学家们学习在培养皿内培养小鼠和人类胚胎里发现的多能干细胞,也因而掌握了所需工具,研究哪些基因和途径是管控这种细胞状态的维持的 [4 , 5]。科学家们还发现了是什么触发所有的特殊细胞(例如形成皮肤、心脏和大脑的细胞)偏离了原有的多能性。处于基因网路的核心的,是一些结合基因组 DNA 之中的特定区域、控制基因是开是关的分子开关掣。SOX2 和 OCT4 就是这些开关掣当中的两个极为重要的版本。SOX2 是一个基因家族的一部分,这个基因家族的创始成员位于 Y 染色体上,作用是性别决定。在原子分辨率下,SOX2 蛋白乃充当一个分子楔子,负责结合和松开 DNA,从而开启基因的表达 [6]。OCT4 是一种来自所谓 POU 家族的多功能模组化蛋白,可以重新排列并改变其与 DNA 结合的方式,从而可以容纳更广泛的 DNA 序列集 [7]。如果 SOX2 和 OCT4 受到突变或丰度改变的干扰,多能干细胞将无法正常发挥作用 [8-10]。2006年,日本科学家山中伸弥得出一项突破性的发现,就是不必破坏胚胎,也都可以获得多能干细胞。我们可以在分化的细胞中引入并强制表达四个基因,这些基因能够促使分化的细胞回复到多能干细胞的胚胎状态 [11]。毫不意外地,SOX2 和 OCT4 是这种神奇基因混合物的一部分,这个基因混合物触发了一个恢复发育、形成我们现在所说的诱导性多能干细胞(iPS 细胞)的程序(图 2)。山中伸弥博士的发现引发了科学界的一场地震,许多科学家开始使用这项技术。现在,我们可以从小鼠、人类以至许多其他动物的皮肤、血液和尿液中,提取细胞,以便制造 iPS 细胞。山中伸弥博士凭著这项突破性技术,荣获 2012 年诺贝尔奖。因为这项技术之故,使得对生物学最基本概念进行的研究激增,并提供了以一种全新方式研究人类疾病的机会,进而激发科学界针对一些最具危害性的疾病展开一系列临床试验。
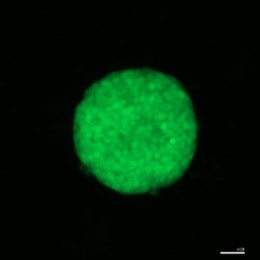
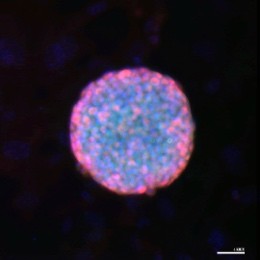
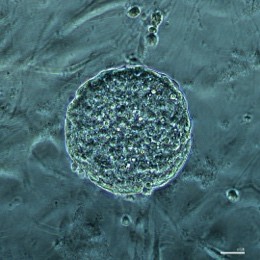
图2:— 显微镜下显示的小鼠诱导性多能干细胞 (iPSC) 集落,当中有多能性标记蛋白 Oct4(绿色)和 Sox2(红色)的染色。影像由高雅博士拍摄。
我们的干细胞里的基因比我们想像的更古老
我们的实验室被 iPS 技术提供的机会所深深吸引。我们对于驱使细胞身份发生变化的分子特别有兴趣。我们试图了解山中因子如何引导将特化细胞转变为非特化 iPS 细胞所需的巨大变化(这种非特化 iPS 细胞能够自我复制增殖并形成身体的所有其他细胞,甚至能够创造出完整的小鼠)。在我们探索是什么使得 SOX2 和 OCT4 如此独特的过程中,我们与德国马尔堡市马普土壤微生物研究所 (Max Planck Institute of Terrestrial Microbiology) 的 Mathias Girbig 博士和 Georg Hochberg 博士以及英国伦敦玛丽王后大学的 Alex de Mendoza 博士合作,著手勾画它们的进化起源。有关的科学文献显示,SOX 和 POU(及其重要成员 OCT4)家族属于动物特有的基因家族。SOX 和 POU 基因的发明是否从单细胞原生生物转变为多细胞动物这个演化的关键性一步?为研究这个问题,我们接触过曾经发表关于动物演化和动物基因库的甚具影响力研究的 Alex de Mendoza 博士。我们想知道早期动物的 SOX 和 POU 基因是什么样的,以及它们是如何成为干细胞的关键角色的。de Mendoza 博士再次回顾了是否只有动物具有 SOX 和 POU 的问题。最近的研究发现了一些新的原生生物物种,并且报道揭露了它们的基因序列。让我们感到意外的是,透过进一步分析这些原生单细胞生物的基因序列,与传统上所认为的相反,我们发现一些单细胞亲戚含有与我们的 SOX2 和 OCT4 高度匹配的 SOX 和 POU 基因序列。由于它们并未在所有领鞭毛虫或丝虫类物种之中被发现,它们以往没有被检测出来。此前,只有两种领鞭毛虫物种被用作为科学上的模范,科学家对其进行了深入研究。无独有偶,这两个物种都没有 SOX 和 POU。然而,领鞭毛虫和丝虫纲里较不知名的成员似乎会产生真正的 SOX 和 POU。我们对这项发现大为振奋,并在香港大学生物医学学院的实验室对其进行了研究。我们想将它们的功能与多能性明星组合 SOX2 和 OCT4 进行比较。
7 亿年前的 Ur-Sox 可用来制造小鼠干细胞
我们首先合成出 SOX 和 POU 基因,然后采用有关技术来生产它们的蛋白质产物,从而检查它们是否会结合 DNA 以及如何结合 DNA。富有才华、孜孜不倦的生物化学家 陈培文博士当时正在港大医学院攻读博士学位的最后阶段,她毅然接受了这项挑战。她发现,原生生物 SOX 可以牢固地结合与我们的 SOX2 相同的 DNA 序列。这就带出了下一个问题:是否单凭这种生物化学特性,就可以让原生生物 SOX 复制 SOX2 的功能,从而制造出 iPS 细胞?在香港大学蛋白质与细胞工程实验室 (@pacelab) 攻读博士学位期间已成为干细胞生物学和复杂 iPS 技术的专家之高雅博士研究著重于这个问题。在哺乳动物中,只有 SOX2 及其最接近的家族蛋白具备制造 iPS 细胞之能力,但此外 20 多个 SOX 家族因子中的大多数都不具备这个能力。但是,高博士研究发现,令人惊讶的是,虽然领鞭毛虫 SOX 已经独立进化了数亿年,但它仍能诱导小鼠的 iPS 细胞。验证 iPS 细胞的多能性之试金石,是将这些细胞与小鼠胚胎混合,然后把它们植入到代孕母体之中。结果很令我们惊奇:用领鞭毛虫 SOX 制成的 iPS 细胞能为可存活的嵌合体小鼠提供组织斑块(图 3)。我们的研究结果在《自然通讯》(Nature Communications) 上发表之后,这只体内有斑块的雌性小鼠和其无 iPS 细胞的伴侣变得有名起来,在《华盛顿邮报》、《福布斯》杂志以至另外许多媒体上都有关于他们的报导。领鞭毛虫 SOX 可以像我们多细胞动物的 SOX2 一样制造 iPS 细胞。领鞭毛虫现在就在我们的周围,其演化历史与我们一样久远。正因这样,它们不应该被视为更加原始或更加古老。理想上,我们希望回到过去,研究过去曾经存在的分子。这正是德国马普土壤微生物研究所的演化生物化学家 Georg Hochberg 博士和 Mathias Girbig 博士所能够做到的。他们采用以动物和原生生物 SOX 基因序列制作的家谱树,并使用统计模型,来推断我们的远古祖先里存在哪一种 SOX 基因。藉著这个方法,他们发掘出祖先 Ur-SOX,这是所有动物的 SOX 基因的前身。高博士证明,即使是这种祖先 Ur-SOX 也能产生小鼠 iPS 细胞。属于我们的单细胞高曾先祖的一个假设性细胞似乎包含一种 SOX 因子,该因子完全有能力释放制造现代哺乳动物干细胞所需的遗传程式。这种远古的 Ur-SOX 可能要比干细胞本身还要老,但非常巧合的是,在进化力量组成基因网路,使干细胞发挥作用时,它便已经存在。


图3:— 左边的嵌合体小鼠是由源自 7 亿年前的领鞭毛虫 SOX 基因的 iPS 细胞生成的,这只小鼠有黑色的皮毛斑块和黑色的眼睛。相反,右边的野生小鼠有白色的皮毛和红色的眼睛。照片来自 高雅博士及 Alvin Kin Shing Lee (香港大学比较医学研究中心)。源自我们的研究论文。[12]
POU 基因的变化是否朝向动物的进化过程中的关键事件?
POU 基因的演化历史更为复杂和富有动态。Alex de Mendoza 博士在较不知名的动物亲戚中进行了基因搜寻,其结果也表明,这些基因应该在第一批动物在地球各处游走之前便已经存在。但是,陈培文博士仔细地进行过生化分析,结果显示,领鞭毛虫 POU 与 DNA 的结合方式跟干细胞因子 OCT4 与 DNA 的结合方式大为不同。毫不奇怪地,领鞭毛虫 POU 不能取代 OCT4 来产生小鼠的 iPS 细胞。在朝向动物进化的道路上,POU 基因较大可能经历了进化性适应的步骤。我们不知道那些步骤何时发生、如何发生,但是,我们推测,第一只动物具有一种 POU 因子,这种 POU 因子结合 DNA 和管控基因的方式与领鞭毛虫 POU 的并不相同。至于 SOX 和 POU 因子是否早已在所有动物的祖细胞中形成了密切的伙伴关系,就像 SOX2 和 OCT4 在我们的多能干细胞中那样,这是一个极为有趣但高度推测性的想法。如果是这样的话,进化过程可能利用了两个预先存在的因子,来选择干细胞的主要管控者。Ur-SOX 早在第一只动物出现并且被纳入这个网络之前很久便已经准备好,而 Ur-POU 在进化成为动物的过程中需要更多的调整才能承担这个角色。
我们能否从进化过程学习,改造干细胞来治疗疾病和延缓衰老?
了解生命的历史、了解塑造我们周围的世界的分子构件是如何进化过来的,这本身就十分有趣。除了寻求学术上的兴趣之外,对大自然的研习结果还可以为我们提供解决人类某些负担的工具。一段时间以来,科学家们已在实验室里运用进化的机制,来优化蛋白质和在功能上改变蛋白质。我们有用以强制和加快定向地或随机地产生突变的过程之必要工具。我们可以设计严格的实验,从而选择「最适合」的蛋白质变异体来达到要求的目的。我们可以透过多次连续的重复,来做到这一点,从而在实验室里逐步演化出蛋白质。以这种方式创制的实验室工程设计蛋白现已在生物科技、农业等领域里有无数的应用,并已被用作药物和治疗补充剂。我们还可以利用设计蛋白,更快捷、更高效地将体细胞转化为干细胞。最近,由 OpenAI 创办人 Sam Altmann 提供 1 亿 8,000 万美元支持的人工智能初创公司 Retro Biosciences [13] 也加入了这一行列,并且已发表了 SOX2 和 KLF4 的人工版本。他们的人工智能算法的训练方式,是透过比较许多蛋白质序列以及学习其自然进化来进行的。他们希望利用他们的人工智能修饰蛋白,来逆转与年龄相关的疾病。多年以来,我们的实验室一直利用实验室进化,来促进各种干细胞的产生。我们相信,采用经重新设计的蛋白质,能够帮助我们研究老化、建立疾病模型、实现物种保护,以及产生具有更高品质的干细胞。我们可以产生能够转化为更多种类的组织甚至细微器官的干细胞。我们希望学会使衰老的干细胞产生真实的细胞,以便捕捉在年龄相关疾病里出现的问题。我们甚或能够利用细胞重新编程的方法,来改变我们体内细胞的身份,从而修复受损的器官。一些科学家更加抱有大胆的希望,希望我们能减缓甚至停止老化带来的负担。在实验室和动物体内操纵细胞的过程中,山中因子和相关分子发挥著关键性角色。从进化中学习,以便回到过去,复活古老的蛋白质,并且以此作为指引,从头开始制造全新的蛋白质,将能帮助我们优化制造我们用以研究衰老问题并最终治疗不同疾病的细胞的因素。
图 4:— 透过祖先 Ur-Sox 寻找动物进化的根源(绘图:杨思颖)
研究论文:
Gao, Y., Tan, D. S., Girbig, M., Hu, H., Zhou, X., Xie, Q., Yeung, S. W., Lee, K. S., Ho, S. Y., Cojocaru, V., Yan, J., Hochberg, G. K. A., de Mendoza, A., & Jauch, R. (2024). The emergence of Sox and POU transcription factors predates the origins of animal stem cells. Nat Commun, 15(1), 9868. https://doi.org/10.1038/s41467-024-54152-x
参考资料︰
- Maehle, A.H., Ambiguous cells: the emergence of the stem cell concept in the nineteenth and twentieth centuries. Notes Rec R Soc Lond, 2011. 65(4): p. 359-78.
- Levit, G.S., et al., The biogenetic law and the Gastraea theory: From Ernst Haeckel's discoveries to contemporary views. J Exp Zool B Mol Dev Evol, 2022. 338(1-2): p. 13-27.
- Droscher, A., Images of cell trees, cell lines, and cell fates: the legacy of Ernst Haeckel and August Weismann in stem cell research. Hist Philos Life Sci, 2014. 36(2): p. 157-86.
- Evans, M.J. and M.H. Kaufman, Establishment in culture of pluripotential cells from mouse embryos. Nature, 1981. 292(5819): p. 154-6.
- Thomson, J.A., et al., Embryonic stem cell lines derived from human blastocysts. Science, 1998. 282(5391): p. 1145-7.
- Tan, D.S., et al., SOX17 in cellular reprogramming and cancer. Semin Cancer Biol, 2020. 67(Pt 1): p. 65-73.
- Malik, V., D. Zimmer, and R. Jauch, Diversity among POU transcription factors in chromatin recognition and cell fate reprogramming. Cell Mol Life Sci, 2018. 75(9): p. 1587-1612.
- Masui, S., et al., Pluripotency governed by Sox2 via regulation of Oct3/4 expression in mouse embryonic stem cells. Nat Cell Biol, 2007. 9(6): p. 625-35.
- Tapia, N., et al., Dissecting the role of distinct OCT4-SOX2 heterodimer configurations in pluripotency. Sci Rep, 2015. 5: p. 13533.
- Malik, V., et al., Pluripotency reprogramming by competent and incompetent POU factors uncovers temporal dependency for Oct4 and Sox2. Nat Commun, 2019. 10(1): p. 3477.
- Takahashi, K. and S. Yamanaka, Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors. Cell, 2006. 126(4): p. 663-76.
- Gao, Y., et al., The emergence of Sox and POU transcription factors predates the origins of animal stem cells. Nat Commun, 2024. 15(1): p. 9868.
- RetroBiosciences. 2025; Available from: https://www.retro.bio/.
作者:
香港大学医学院生物医学学院教授及干细胞转化研究中心首席研究员Ralf Jauch教授
鸣谢
我们衷心感谢Mathias Girbig博士、 Alex de Mendoza博士、陈培文博士、高雅博士以及 Hannah Lam 对本专题文章的宝贵意见。
2025年3 月
