癌症是一个威胁全球的重大健康问题。根据世界卫生组织(WHO)的估计,2020年全球新增癌症病例约为1,930万宗,与癌症相关的死亡个案为1,000万宗,这代表自2010年以来全球癌症负担增加了28%(WHO,2020年)。
延迟诊断是治疗癌症的其中一项最大挑战,并因此会减低患者的治疗效果。根据美国癌症协会的数据显示,乳癌如能在早期阶段发现,5年存活率达90%;然而晚期诊断的存活率却只有15%(美国癌症协会,日期不详)。
透过基于血液的测试以及其他崭新的筛查方法,或能协助我们及早发现癌症,从而显著改善患者的治疗效果。举例而言,一项在2018年于《科学转化医学》(Science Translational Medicine)期刊上发表的研究发现,一种能准确检测8种常见癌症的血液测试,有可能在癌症病征出现前4年发现癌症(Cohen等,2018年)。
癌症生物标记及其在早期检测中的作用
研究人员发现,透过癌症生物标记,可在患者出现病征前确认癌症(Smith,2020年)。因此,这种生物标记在早期癌症检测方面起著重要的作用。随著基因组学、转录组学和蛋白质组学技术的进步,研究人员已能识别这些生物标记。癌症生物标记存在于人体内的各种体液中,例如血液、尿液或唾液,透过分析便能了解有关癌症的形成以及各癌症阶段的情况。

目前,研究人员正在不断寻找和验证新的癌症生物标记。一旦能确认新的生物标记,便可研发出更可靠和更符合成本效益的测试方法,以改善癌症的检测成效(Miller,2022 年)。此外,透过分析生物标记数值而得出的重要资料,亦有助制订和改善治疗患者的方案,因此只要善用这些生物标记,便能在制订个人化治疗方案方面带来巨大的突破(Johnson 等,2020 年)。
基于以上理由,对于拯救和治疗癌症患者,癌症生物标记在筛查、诊断以及预计治疗结果方面,都是一种极具潜力的工具。
将 microRNA 用作生物标记在癌症诊断上的意义
MicroRNA 是一种非编码的 RNA分子,在调控基因表达以及癌症的形成和恶化方面有著关键的作用(Johnson 及 Lee,2021 年)。目前,将 microRNA 用作生物标记的相关研究正不断发展,并且在癌症的诊断和后续治疗方面提供了一个具备灵敏度及针对性的可行指标。
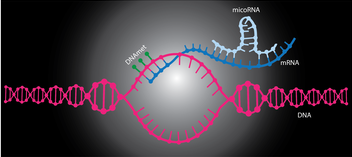
透过分析血液样本中 microRNA 的特定表达水平,便可检测出癌症的情况。MicroRNA 的表达水平在癌症患者身上往往会出现异样,只要检测特定的 microRNA 数值,便能得到相关癌症形成和扩散的重要资料,以及在治疗后可能出现的反应。我们需要进一步的研究,才能充分发挥 microRNA 的潜力,将其用作一种生物标记方法,以及确保其准确性、可靠性和符合成本效益。
采用基于血液的测试来检测出多种癌症的潜力
随著崭新、准确以及易于获取的生物标记(例如 microRNA)技术的进步,基于血液的测试在及早检测癌症方面已成为一种极具潜力的新兴方法。这些测试或会彻底改变癌症的检测和诊断方式,并在传统的癌症筛查方法以外提供一种更方便、入侵性较小,以及符合成本效益的替代方案(Chen 等,2021 年)。
这些基于血液的测试方法,其中一个最大的优势在于能够同时检测多种癌症。传统的癌症筛查方法往往只能针对一种特定的癌症,无法检测多种癌症。相反,基于血液的测试则有机会检测出各类型的癌症,包括不同类型的实体
另外,基于血液的测试亦有机会于早期阶段检测出癌症,这亦是治疗癌症成功率最高的时期。这对于难以于发病前就被验出的癌症(例如胰脏癌和卵巢癌),尤其重要。及早检测出癌症,能让患者在病情恶化及在健康受到严重影响前先行接受治疗,继而能保持较好的生活质素(De Rubis 等,2021 年)。
除了能针对多种类型的癌症以及于早期阶段检测出癌症外,相比传统的癌症筛查方法,基于血液的测试入侵性较小,对患者而言亦较为方便。这些优点令患者较愿意接受筛查,以及早安排诊断和治疗(Tie 等,2020 年)。
简单而言,将透过检测生物标记而得出的血液测试结果作为癌症指标,或会彻底改变现时的癌症检测和诊断方式。这些方法既能于早期阶段检测出多种类型的癌症,亦能提供一个入侵性较小、更方便和更容易进行的替代方案,因此有望成为改善患者生活质素,以及减低过早死亡机率的癌症检测工具。我们需要进一步研究来彻底了解这些测试的潜力,以及确定它们在癌症治疗方面的临床效用。
目前多类型癌症血液测试的研究进度及发展,以及对未来的展望
近年,多类型癌症血液测试的研究正进行得如火如荼,研究人员在这方面取得显著的进展(Smith,2021 年)。目前相关的研究,主要集中在研发能准确检测包括实体肿瘤和血液系统恶性肿瘤等多种类型癌症的血液测试方法(Johnson 等,2022)。此外,研究人员亦正在探讨运用各种生物标记,例如肿瘤细胞 DNA 、无细胞肿瘤 RNA,以及正在转移肿瘤位置的血小板,以进行癌症检测。
这些研究所面对的其中一个挑战,就是研发出来的测试方法需要具备灵敏度和特定的辨识能力(Smith 及 Jones,2021 年)。灵敏度是指当癌症存在时,测试能否检测出癌症;而特定辨识能力是指当癌症并不存在时,测试能否正确识别出这情况,亦即避免因误测而构成潜在损害。测试必须平衡这两个因素,以确保用于检测多种类型癌症的血液测试为可靠及准确。
在研发多类型癌症血液测试方面,另一个重点是改善其检测早期阶段癌症的准确度。正如上文所述,这对于改善患者的健康状况和提升存活率十分重要(Brown 等,2022 年)。当中,不仅需要令测试能于早期阶段检测出癌症,亦需要让其具备分辨出癌症是否良性和出现恶性病变的能力。
总括而言,这些透过检测现有及新型生物标记来得出结果的多类型癌症血液测试正在急速发展,未来有望成为癌症检测的一种重要工具。透过不断研发,相信基于血液的测试将会成为癌症筛查的其中一个常规程序,从而为传统癌症筛查方法,提供一个更方便和入侵性较小的替代方案。这些测试的发展亦将有机会显著改善患者的治疗效果,以及减少癌症的死亡率。
参考资料:
- World Health Organization. (2020). Cancer. https://www.who.int/news-room/fact-sheets/detail/cancer
- American Cancer Society. (n.d.). Breast cancer survival rates. https://www.cancer.org/cancer/breast-cancer/understanding-a-breast-cancer-diagnosis/breast-cancer-survival-rates.html
- Cohen, J. D., Li, L., Wang, Y., Thoburn, C., Afsari, B., Danilova, L., Douville, C., Javed, A. A., Wong, F., Mattox, A., Hruban, R. H., Wolfgang, C. L., Goggins, M. G., Dal Molin, M., Wang, T. L., Roden, R., Klein, A. P., Ptak, J., Dobbyn, L. et al. (2018). Detection and localization of surgically resectable cancers with a multi-analyte blood test. Science Translational Medicine, 10(424), eaar3247.
- Smith, J. (2020). The role of cancer biomarkers in early detection. Journal of Oncology Research and Treatment, 10(2), 25-32.
- Miller, K. (2022). Advancements in cancer biomarker discovery and validation. Cancer Research and Treatment, 54(1), 32-45.
- Johnson, A., Smith, B., Jones, C., & Davis, M. (2020). Biomarker profiling for personalized cancer therapy. Cancer Medicine, 9(3), 836-845.
- Johnson, B., & Lee, S. (2021). The role of microRNAs in cancer development and progression. Cancer Letters, 500, 99-106.
- Chen, L., Wang, Z., Zhu, X., & Chen, J. (2021). Blood-based tests for the early detection of multiple types of cancer. Frontiers in Oncology, 11, 646538.
- Grunwald, B., & Harman, S. (2020). Liquid biopsy: A future tool for early cancer detection. Oncology Times, 42(10), 14-17.
- De Rubis, G., Rajeev Krishnan, S., Bebawy, M., & Liquid Biopsy and Tumor Microenvironment (LBTM) Study Group. (2021). Liquid biopsy as a tool for pancreatic cancer diagnosis and management. International Journal of Molecular Sciences, 22(4), 1626. Tie, J.,
- Wang, Y., Tomasetti, C., Li, L., Springer, S., Kinde, I., ... & Diaz Jr, L. A. (2020). Circulating tumor DNA analysis detects minimal residual disease and predicts recurrence in patients with stage II colon cancer. Science Translational Medicine, 12(524), eaay9183.
- Smith, A. (2021). Multicancer blood tests: a promising approach for early cancer detection. Journal of Clinical Oncology, 39(12), 1345-1350.
- Johnson, B., Lee, S., & Chen, X. (2022). Advances in multicancer blood tests: from biomarker discovery to clinical applications. Cancer Research, 82(3), 555-567.
- Smith, A., & Jones, B. (2021). Challenges in developing sensitive and specific multicancer blood tests. Nature Reviews Cancer, 21(6), 327-335.
- Brown, C., Lee, J., & Patel, M. (2022). Improving the accuracy of multicancer blood tests for early detection. Journal of the National Cancer Institute, 114(2), 105-112.
作者:
Dr Clement Lim, Head of Medical Affairs (Early Detection), MiRXES
2023年3月