堕进幻想空间
癌症对人类来说无疑是其中一种最可怕的疾病,它被定义为一种细胞失控地进行分裂的病症[1] 。除了手术外,传统的治疗方法还包括放射治疗及化学治疗,原意是选择性地杀死癌细胞,但是这两种疗法都有同时错误杀死健康细胞的可能,所以时常带来不良的副作用[2] 。幸好,免疫疗法(immunotherapy )近来的突破让我们可以借用 自身的免疫系统,更精确地对抗癌症。让我们进入幻想世界,认识一下广为人知的嵌合抗原受体T细胞疗法(chimeric antigen receptor T cell (CAR-T cell) therapy )吧:那是一只我们特意创造来消灭癌症的合成怪物1。这个疗法的概念就是从病人身体提取一种叫T细胞的免疫细胞,然后在体外把它们基因改造成嵌合抗原受体T细胞(CAR-T细胞),再把已转化的细胞注射回病人的身体内。利用得来的新能力,CAR-T细胞能辨认并攻击癌细胞,因此将它们形容为活生生的药物2也绝不夸张!
基本知识—工作中的免疫细胞!
CAR-T细胞是基于我们现时对免疫细胞的认识而制成的。免疫细胞是身体对付感染和疾病自然防御机制的一部分。以下是关于与疗法相关的免疫细胞的一些基本知识。
事实一:疗法所用到的T细胞为细胞毒性T细胞
又被称为「杀手T细胞(killer T cells )」,我们可以从它的名字中猜想到其功能就是杀掉其他细胞(它对「细胞」有「毒性」)。细胞毒性T细胞通常会杀死受损的细胞,因为它们继续存在对身体并不是一件好事,例如受病毒感染的细胞,它们很有可能被劫持而协助复制病毒。T细胞的主要工作是要分辨岀受损细胞和健康细胞,杀掉前者并放过后者。辨识工作全靠T细胞受体(T-cell receptor )负责,它能够识别只出现在受损细胞表面、而不存在于健康细胞的抗原。当T细胞受体与抗原结合时,它会发送讯号活化T细胞,让T细胞通过引发细胞溶解(cell lysis )3来杀死受损细胞。
事实二:抗体由另一种免疫细胞— B细胞所制造
从B细胞分化而成的浆细胞会产生称为抗体的蛋白质。抗体的形状像英文字母「Y 」,它拥有的标志性的功能就是能用「Y 」字的两个尖端专一地与相应的抗原结合。那对尖端被称为可变区,不同抗体之间的可变区差异很大,它决定了一个抗体的目标抗原,意义上可谓赋予了抗体一个「身份」。相比之下,余下的部分被称为恒定区;相同的恒定区可以出现在不同抗体中。
一旦与抗体结合,抗原本身(可能是毒素),或是表面带有抗原的物体(多为不受欢迎的东西,例如癌细胞或病原体等)将被其他免疫细胞识别,然后免疫细胞可能透过吞噬作用(phagocytosis )把它们整个吞下。然而,这个系统并不完美;就癌细胞而言,免疫系统并不是时常能够辨认出它们就是我们身体中的敌人。
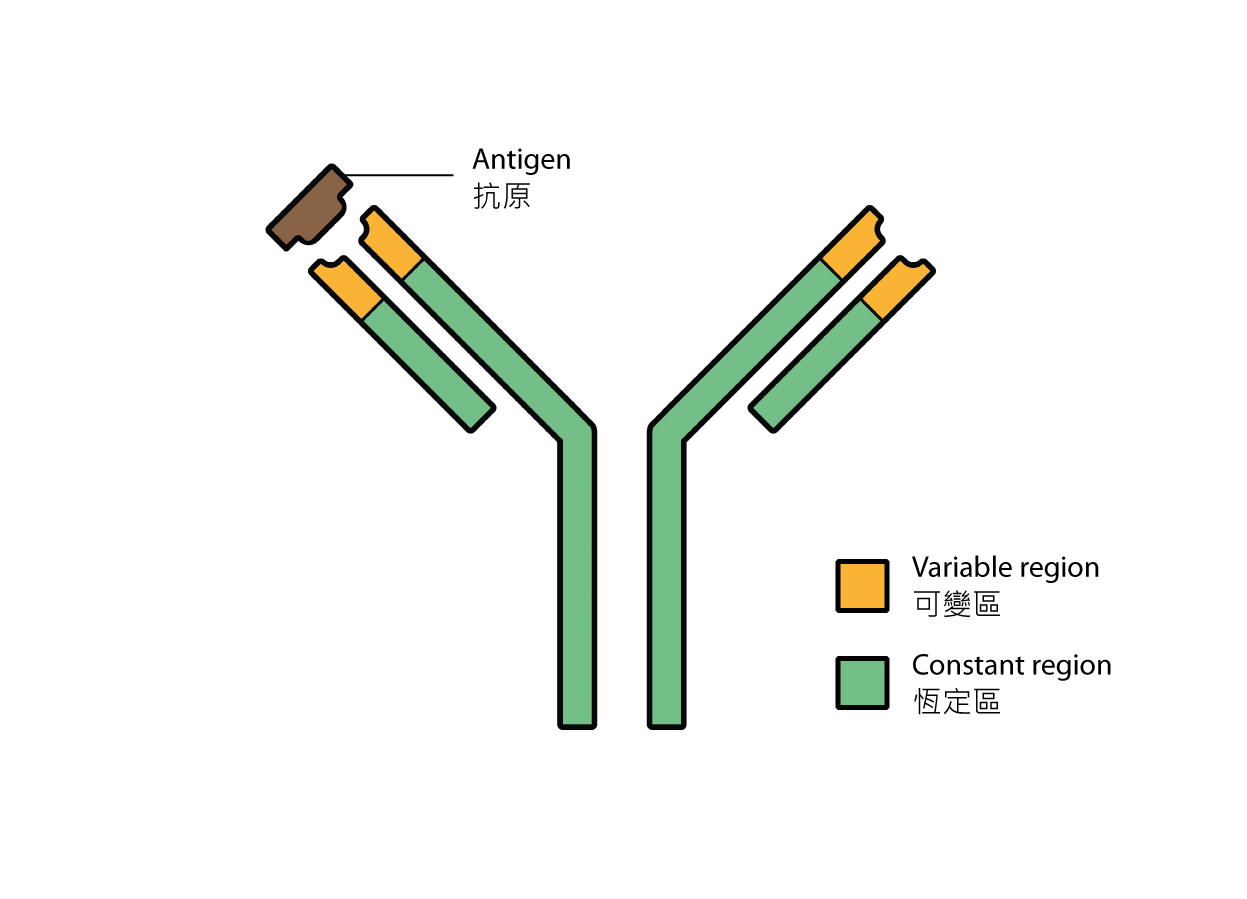
图一 抗体的结构
强大的合成怪物— CAR-T细胞
事实上,CAR-T细胞中「chimeric 」一字源于希腊神话中一只会喷火的混种怪物—凯美拉(Chimera )。它是狮子、山羊与蛇的混合体,而CAR-T细胞亦名副其实是细胞毒性T细胞和抗体的混合体。CAR-T细胞利用嵌合T细胞受体(chimeric T-cell receptor )来识别癌细胞,「嵌合」二字形容受体是由数个蛋白质结构域(蛋白质的构成部分)融合而成,当中的选用的结构域取自不同蛋白质,各有独特的功能。
像其他受体(或感受器)一样,嵌合抗原受体4共有三个结构域:细胞外域(在细胞外)、跨膜域(嵌在细胞膜中)和细胞内域(在细胞内)[3] 。在这样的结构下,嵌合抗原受体的细胞外域来自抗体的可变区,它能专一地跟与肿瘤相关的抗原结合。在癌细胞表面往往有大量与肿瘤相关的抗原,尽管它们并不一定是癌细胞独有的。科学家期望所选择的细胞外域可以将CAR-T细胞引导至癌细胞。至于跨膜域,它通常来自现有的受体;这个结构域的作用是将整个嵌合抗原受体固定于细胞膜。最后还有细胞内域,当中包含普通T细胞受体的细胞内讯号传导结构域(intracellular signaling domains ),以及其他协同刺激受体的细胞内讯号传导结构域。简单而言,当细胞外域跟与肿瘤相关的抗原结合时,它还可以活化CAR-T细胞,从而令癌细胞溶解。
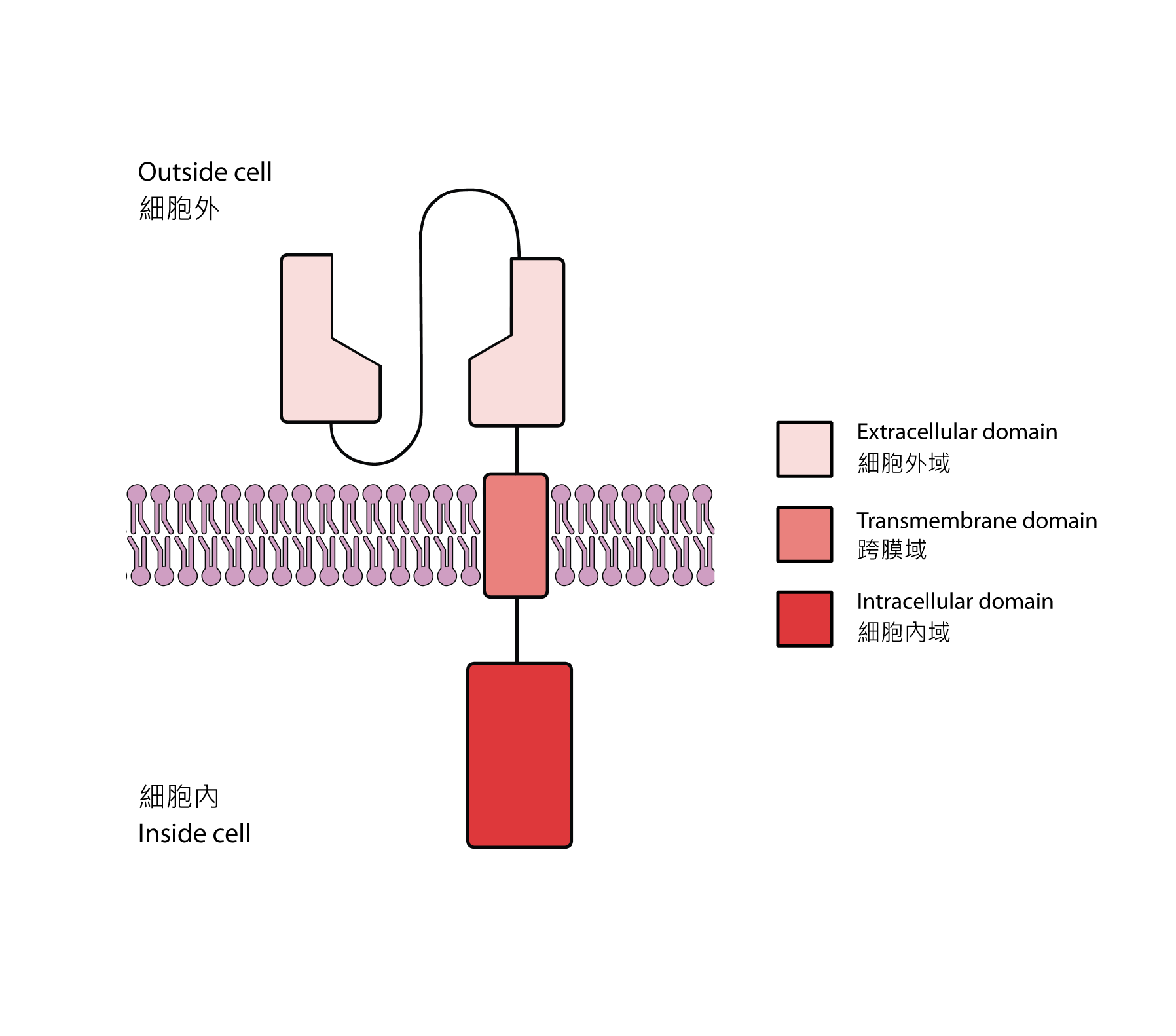
图二 嵌合抗原受体的结构
由零开始「组装」我们的武器
那我们究竟是怎样制造出CAR-T细胞的呢?当选定了合适的蛋白质结构域后,我们会在实验室里以基因工程技术,把这些结构域相应的基因序列串连起来,并将其合并到从患者身体抽取的T细胞当中的基因组内。这些细胞现在能够根据我们输入的「指令」(DNA序列),生产出特别订制的「武器」(之前提及的嵌合受体),制造出CAR-T细胞。此后CAR-T细胞会重新注射回患者体内,让其发挥「活体药物」的作用。
疗效与未来挑战
由于CAR-T细胞具有治疗癌症的潜力,科学家已经进行了不少临床试验来测试其对各种类型癌症的效用。根据芝加哥大学的一项研究[4] ,对于部分癌症,以CAR-T细胞治疗并达至长期缓解(remission )的成功率目前为30%至40% 。
尽管它功能强大,要使CAR-T细胞疗法变得完善并非易事。CAR-T细胞疗法面对的其中一个挑战就是「on-target off-tumor toxicity (击中目标但并非肿瘤毒性)」。如前文所述,与肿瘤相关的抗原并非癌细胞独有,它们亦可能存在于健康细胞表面。这有机会导致安全问题,因为CAR-T细胞可能错误地盯上健康细胞上的抗原。另一个挑战在于癌细胞所在的肿瘤微环境(tumor microenvironment ),它可能会抑制CAR-T细胞的功能[5] 。直到现在,科学家仍在努力克服这些弱点,而一些设计更先进的CAR-T细胞经常都会出现。一些显著的改进包括在CAR-T细胞中加上逻辑闸(logic gate )5以提高其专一性和安全性[6] ;亦有一些透过施以额外分子,例如免疫检查点抑制剂(immune checkpoint inhibitor ),来制衡免疫抑制的肿瘤微环境,从而防止癌细胞通过「欺骗」CAR-T细胞而避过其攻击[7] 。
什么是免疫检查点抑制剂?
从上文中,你会了解到抗原一旦与T细胞受体结合,T细胞就会被活化而杀死癌细胞。然而,科学家却发现了一个名为「免疫检查点(immune checkpoint)」的额外的调节器,它可以推翻上述的决定,而放生目标细胞;它是一个相反的机制,原意是避免免疫反应的过度激发[8]。利用这一发现,崭新的检查点抑制剂免疫疗法采用抑制剂来堵住癌细胞所表达的检查点。在理想情况下,没有癌细胞再能逃过T细胞的攻击。这使其发现者赢得了2018年诺贝尔奖。
总结
有着「程式控制癌症杀手(programmed cancer killer )」的美誉,CAR-T细胞近年来受到广泛关注。尽管我们以往都按照传统地偏向使用化学性药物,CAR-T细胞却向我们展示了一类崭新的「活体」药物。包括CAR-T细胞在内的免疫疗法与其他疗法不同之处,在于这类疗法是利用我们自身的免疫系统来对抗疾病。事实上,免疫系统一直是我们的忠实守护者,不知不觉间全天候地保护着我们的身体。借着把它们用创新方法升级,它可以用来杀死难以对付、叛变的癌细胞。希望这个疗法在将来能变得更有效和副作用能大大减少,使人类可以更有效地治疗癌症。
1 编按:「Chimera 」在英文有多重意思,原指希腊神话一只会喷火、由狮子、山羊和蛇合成的怪兽,引伸义为「幻想、空想」,后来被借用至生物学上。作者在英文原文中用了语带双关的手法。
2 编按:CAR-T细胞在英文普遍被形容为「living drug 」。
3 T细胞可以透过释放一些会戳破细胞膜的蛋白质,使目标细胞爆裂而死,这称为细胞溶解。
4 CAR-T细胞中的嵌合T细胞受体(chimeric T-cell receptor )更常被称为嵌合抗原受体(chimeric antigen receptor/CAR );两者指的是同一样东西,只是从不同角度命名而已— T细胞上的受体,或是与抗原结合的受体。
5 逻辑闸执行逻辑运算,并根据其接收的输入讯号产生相应的输出讯号。
References:
[1] Shiel, W. C. Jr. (n.d.). Medical Definition of Cancer. Retrieved from https://www.medicinenet.com/script/main/art.asp?articlekey=2580 [2] Cancer Research UK. (2020, June 10). How chemotherapy works. Retrieved from https://www.cancerresearchuk.org/about-cancer/cancer-in-general/treatment/chemotherapy/how-chemotherapy-works [3] Ghorashian, S., Pule, M., & Amrolia, P. (2015). CD19 chimeric antigen receptor T cell therapy for haematological malignancies. British Journal of Haematology, 169(4), 463–478. doi: 10.1111/bjh.13340 [4] Bartosch, J. (2019, October 17). Three years after CAR T-cell therapy for lymphoma, patient still cancer-free. Retrieved from https://www.uchicagomedicine.org/forefront/cancer-articles/a-walking-miracle-car-t-cell-therapy [5] Tormoen, G. W., Crittenden, M. R., & Gough, M. J. (2018). Role of the immunosuppressive microenvironment in immunotherapy. Advances in Radiation Oncology, 3(4), 520–526. doi: 10.1016/j.adro.2018.08.018 [6] Morsut, L., Roybal, K. T., Xiong, X., Gordley, R. M., Coyle, S. M., Thomson, M., & Lim, W. A. (2016). Engineering Customized Cell Sensing and Response Behaviors Using Synthetic Notch Receptors. Cell, 164(4), 780–791. doi: 10.1016/j.cell.2016.01.012 [7] Goodman, A. (2018, December 25). Combining a Checkpoint Inhibitor with CAR T-Cell Therapy May Augment Immune Response. Retrieved from https://www.ascopost.com/issues/december-25-2018/combining-a-checkpoint-inhibitor-with-car-t-cell-therapy-may-augment-immune-response/ [8] The Nobel Prize. (2018, October 1). Press release: The Nobel Prize in Physiology or Medicine 2018. Retrieved from https://www.nobelprize.org/prizes/medicine/2018/press-release/
作者︰ 刘以轩先生 《科言》学生编辑 香港科技大学
2021年3月